Resumen breve
Este video explica cómo balancear ecuaciones químicas. Se explica que una ecuación química representa una reacción química, donde los reactivos se transforman en productos. Para balancear una ecuación, se deben tener la misma cantidad de átomos de cada elemento en ambos lados de la ecuación. Se utiliza un método para balancear la ecuación, multiplicando los coeficientes de cada molécula por un número entero.
- Se explica el concepto de balancear ecuaciones químicas.
- Se muestra un ejemplo de una ecuación química no balanceada.
- Se explica cómo balancear la ecuación utilizando coeficientes.
¿Qué es balancear ecuaciones químicas? [0:00]
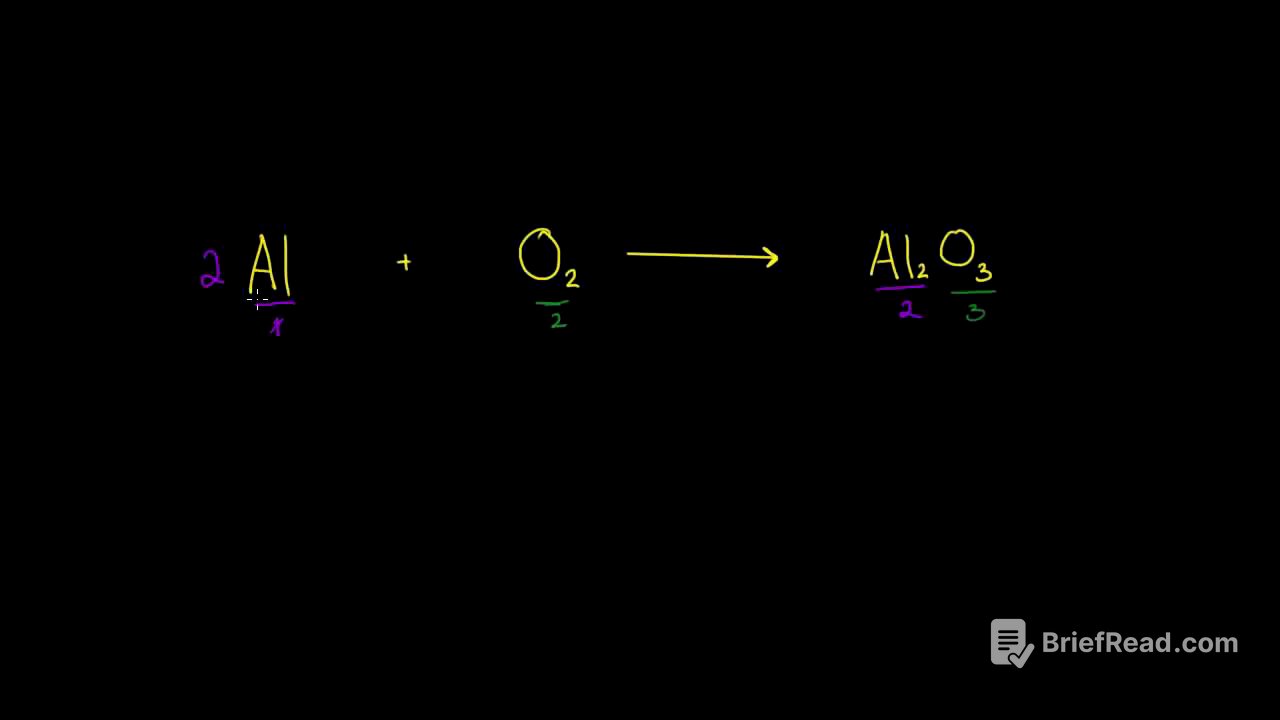
El video comienza explicando qué es una ecuación química. Se muestra un ejemplo de una reacción química entre aluminio y oxígeno, donde se forma óxido de aluminio. Se explica que la ecuación química no está balanceada porque hay diferentes cantidades de átomos de aluminio y oxígeno en los reactivos y productos.
Balanceando la ecuación [1:13]
Se explica que para balancear la ecuación, se deben ajustar los coeficientes de cada molécula. Se muestra cómo se puede multiplicar la molécula de aluminio por 2 y la molécula de oxígeno por 1.5 para obtener la misma cantidad de átomos de aluminio y oxígeno en ambos lados de la ecuación. Se explica que no se pueden usar números decimales como coeficientes, por lo que se multiplica toda la ecuación por 2 para obtener coeficientes enteros. Se verifica que la ecuación está balanceada contando los átomos de cada elemento en ambos lados de la ecuación.