Resumen breve
Este video explica las reacciones redox, que son reacciones químicas que involucran la transferencia de electrones entre sustancias. La oxidación es la pérdida de electrones, mientras que la reducción es la ganancia de electrones. El video explica cómo identificar la oxidación y la reducción utilizando el número de oxidación, que es la carga que tiene o tendría un átomo en un compuesto. El video también destaca que las reacciones redox son fundamentales en muchos procesos, como la producción de energía en nuestro cuerpo y la producción de baterías.
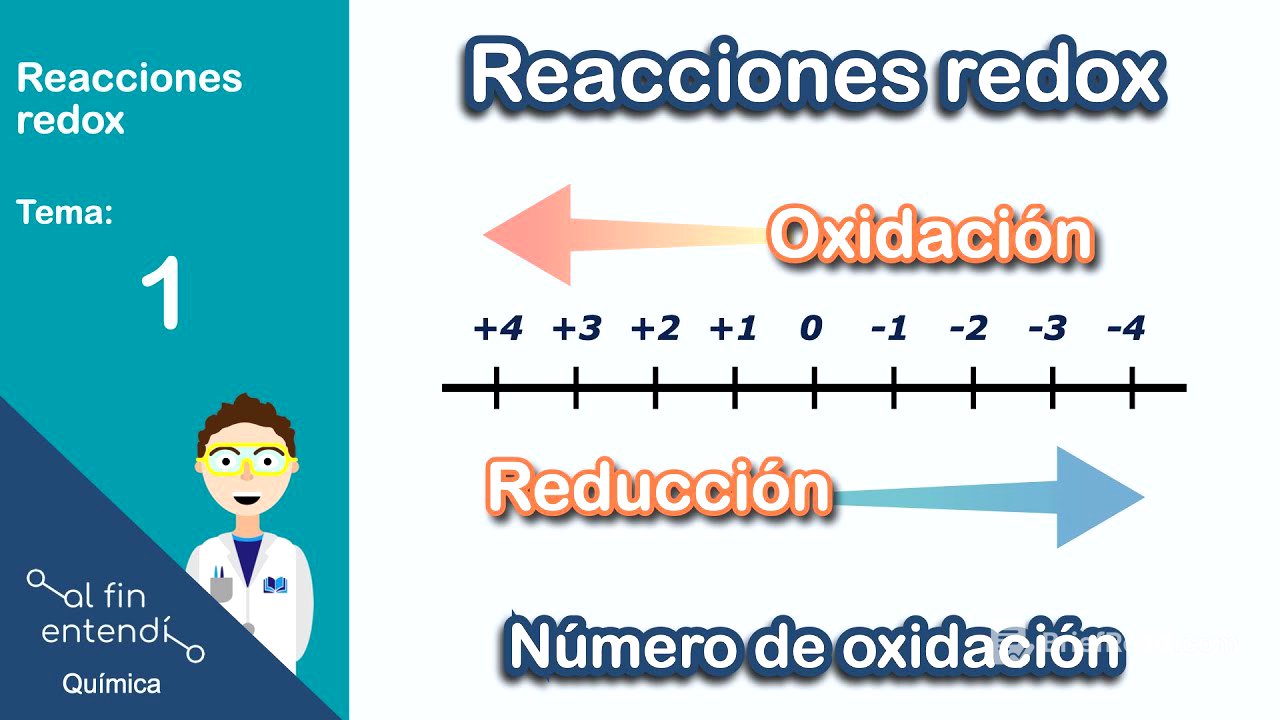
- Las reacciones redox son reacciones químicas que involucran la transferencia de electrones.
- La oxidación es la pérdida de electrones, mientras que la reducción es la ganancia de electrones.
- El número de oxidación se utiliza para identificar la oxidación y la reducción.
Importancia de las reacciones redox [0:00]
Este capítulo introduce el concepto de reacciones redox y su importancia en la química. Se explica que las reacciones redox son fundamentales para entender una gran cantidad de fenómenos que ocurren a nuestro alrededor, como el funcionamiento de las baterías, el tratamiento de agua potable y la digestión de alimentos. Se menciona que las reacciones redox son más complejas que la simple reacción con oxígeno, y que son esenciales para comprender muchos procesos químicos.
¿Qué es oxidación-reducción? [1:40]
Este capítulo explica en detalle el concepto de oxidación-reducción. Se explica que la oxidación y la reducción ocurren simultáneamente, es decir, cuando una sustancia se oxida, otra se reduce. Se utiliza el ejemplo de la oxidación del hierro para ilustrar este concepto. Se explica que la oxidación es la pérdida de electrones y la reducción es la ganancia de electrones. Se utiliza un ejemplo sencillo de dos átomos para explicar cómo se transfieren los electrones en una reacción redox.
Número de oxidación [3:35]
Este capítulo introduce el concepto de número de oxidación. Se explica que el número de oxidación es la carga que tiene o tendría un átomo en un compuesto. Se utilizan ejemplos de compuestos iónicos y covalentes para explicar cómo se determina el número de oxidación. Se menciona que el número de oxidación puede ser diferente para un mismo elemento dependiendo del compuesto en el que se encuentre.
Identificar oxidación y reducción [6:05]
Este capítulo explica cómo utilizar el número de oxidación para identificar la oxidación y la reducción en una reacción química. Se utiliza el ejemplo de la reacción entre sodio y cloro para formar cloruro de sodio. Se explica que el elemento que se oxida es aquel cuyo número de oxidación aumenta, mientras que el elemento que se reduce es aquel cuyo número de oxidación disminuye. Se explica que el aumento o disminución del número de oxidación no necesariamente implica un cambio de signo, sino que se refiere a un cambio en el valor absoluto del número.
Resumen [10:25]
Este capítulo resume los conceptos clave del video. Se recuerda que las reacciones redox son reacciones químicas que involucran la transferencia de electrones. Se explica que la oxidación es la pérdida de electrones y la reducción es la ganancia de electrones. Se menciona que el número de oxidación se utiliza para identificar la oxidación y la reducción. Se destaca la importancia de las reacciones redox en muchos procesos químicos y biológicos.